盘点丨2019年IVD行业十大热点事件
- 分类:行业动态
- 作者:比扬医疗
- 来源:www.csbeyond.com
- 发布时间:2020-01-05 17:46
- 访问量:
【概要描述】2019年对于IVD行业来说是至关重要的一年,这一年里,医疗器械注册人制度的试点范围不断扩大,多家IVD企业闯关科创板,国家局又发布了新增和修订的免于进行临床试验的体外诊断产品目录......除了这些,还发生了哪些引人关注的热点事件呢? 一、医疗器械注册人制度试点范围扩大 2017年3月,国务院印发《全面深化中国(上海)自由贸易试验区改革开放方案》,医疗器械注册人制度首先在上海自贸区试点。同年1
盘点丨2019年IVD行业十大热点事件
【概要描述】2019年对于IVD行业来说是至关重要的一年,这一年里,医疗器械注册人制度的试点范围不断扩大,多家IVD企业闯关科创板,国家局又发布了新增和修订的免于进行临床试验的体外诊断产品目录......除了这些,还发生了哪些引人关注的热点事件呢? 一、医疗器械注册人制度试点范围扩大 2017年3月,国务院印发《全面深化中国(上海)自由贸易试验区改革开放方案》,医疗器械注册人制度首先在上海自贸区试点。同年1
- 分类:行业动态
- 作者:比扬医疗
- 来源:www.csbeyond.com
- 发布时间:2020-01-05 17:46
- 访问量:
2019年对于IVD行业来说是至关重要的一年,这一年里,医疗器械注册人制度的试点范围不断扩大,多家IVD企业闯关科创板,国家局又发布了新增和修订的免于进行临床试验的体外诊断产品目录......除了这些,还发生了哪些引人关注的热点事件呢?
一、医疗器械注册人制度试点范围扩大
2017年3月,国务院印发《全面深化中国(上海)自由贸易试验区改革开放方案》,医疗器械注册人制度首先在上海自贸区试点。同年12月7日,上海市药监局发布关于实施《中国(上海)自由贸易试验区内医疗器械注册人制度试点工作实施方案》的通知。2018年7月5日,上海药监部门发布公告将试点扩大到上海市全市范围。同时,德赛诊断系统(上海)有限公司的四款生化诊断试剂盒获批,从受理到上市仅用时2个月。2018年8月,试点范围扩大到广东自贸区和天津自贸区。
2019年8月1日,国家药品监督管理局发布《关于扩大医疗器械注册人制度试点工作的通知》,明确医疗器械注册人制度试点范围扩大到北京、天津、河北、辽宁、黑龙江、上海、江苏、浙江、安徽、福建、山东、河南、湖北、湖南、广东、广西、海南、重庆、四川、云南、陕西等21个省、自治区、直辖市。
随着2019年12月19日河南省药监局发布试点工作实施方案,21省/自治区/直辖市的医疗器械注册人制度试点工作实施方案已全部发布,标志着医疗器械注册人制度迈入新阶段!
据了解,截至2019年11月,已有11家企业18个产品通过试点获批上市,其中还有部分产品实现了跨省获批。
二、科创板开市,五家IVD企业闯关
2018年11月5日,中央宣布在上交所设立科创板并试点注册制。2019年6月13日,科创板举行开板仪式。科创板打破了发行市盈率限制,有利于扩大企业首发融资额。
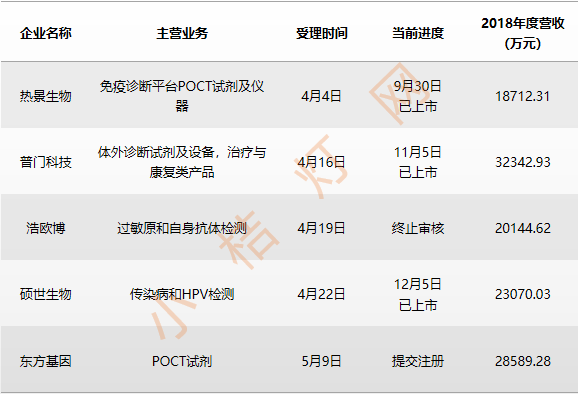
IVD创新企业前期研发投入高,属于资金和技术密集型企业,融资需求大。科创板接受上市申请不到三个月,就有热景生物、普门科技、浩欧博、硕世生物、东方基因等5家IVD企业争相冲击。科创板设置了五套差异化上市指标,上述5家企业均使用了标准一,即市值门槛为十亿元,核心是盈利性。据相关媒体消息,免疫诊断产品提供商科美诊断近日已提交上市辅导备案,拟于科创板上市。
三、新增和修订免于进行临床试验
产品目录
2018年9月,国家药品监督管理局发布了《关于公布新修订免于进行临床试验医疗器械目录的通告》(2018年第94号),涵盖855项医疗器械产品和393项体外诊断试剂产品。2019年12月20日,国家药品监督管理局发布了《关于公布新增和修订的免于进行临床试验医疗器械目录的通告》(2019年第91号),新增148项医疗器械产品和23项体外诊断试剂产品,对48项医疗器械产品和4项体外诊断试剂产品名称和描述进行了修订。
从2014年8月国家药监局第一次发布免临床目录以来,已经涵盖了416项体外诊断试剂产品和54项体外诊断仪器产品。近年来,国家局不断扩大免于进行临床试验体外诊断产品的产品范围,不仅使我国在医疗器械临床试验方面的要求,进一步与国际接轨;而且还降低了成熟度高、风险较低产品临床试验方面的要求,减轻了企业负担,使企业能将更多的精力投入到产品研发和质量提升上;同时也有利于进一步推进基于产品风险的临床评价方式,优化临床试验和审评审批资源,把宝贵的资源投入到临床急需和创新医疗器械产品上去,促进安全有效、风险可控的产品尽快上市,满足人民群众不断提高的用械需求。
四、医疗器械也有了唯一的“身份证”
近年来,医疗器械产业发展迅猛,新技术、新产品层出不穷,产品多样性、复杂性程度不断提升,医疗器械在流通使用环节无码或者一物多码现象普遍,严重影响了医疗器械生产、流通、使用等各环节对医疗器械的精准识别,难以实现有效监督和管理。
医疗器械唯一标识(Unique Device Identification,简称UDI)是医疗器械的身份证,医疗器械唯一标识系统由医疗器械唯一标识、数据载体和数据库组成。为每个医疗器械赋予身份证,实现生产、经营、使用各环节的透明化、可视化,提升产品的可追溯性,是医疗器械监管手段创新和监管效能提升的重要抓手,对严守医疗器械安全底线、助力医疗器械产业高质量发展都将起到积极作用。
国际上,2013年,国际医疗器械监管机构论坛(IMDRF)发布医疗器械唯一标识系统指南。同年,美国发布医疗器械唯一标识系统法规,要求利用7年时间全面实施医疗器械唯一标识。2017年,欧盟立法要求实施医疗器械唯一标识,日本、澳大利亚、阿根廷等国家也相继开展相关工作。
在我国,2012年,国务院印发《“十二五”国家药品安全规划》,要求“启动高风险医疗器械国家统一编码工作”。2016年,国务院印发《“十三五”国家药品安全规划》,要求“构建医疗器械编码体系,制定医疗器械编码规则”。2019年,国务院办公厅印发《深化医药卫生体制改革2019年重点工作任务》,要求“制定医疗器械唯一标识系统规则”。2019年7月1日,国家药监局会同国家卫生健康委联合印发《医疗器械唯一标识系统试点工作方案》,拉开我国医疗器械唯一标识系统建设序幕。
2019年12月5日,上海市药监局、上海市卫健委印发了《上海市推进医疗器械唯一标识系统试点工作方案》的通知,通知显示,上海32家医疗器械企业和12家医疗机构入选第一批试点单位,其中包括罗氏诊断、贝克曼、西门子、雅培等IVD跨国企业。
五、中国首个PD-L1检测试剂盒获批上市
2019年8月30日,Dako North America(代理人:安捷伦科技(中国)有限公司)的PD-L1检测试剂盒(免疫组织化学法)获批上市,这也是国内首个批准上市的PD-L1检测试剂盒。
根据该产品的技术审评报告显示,本试剂盒用于定性检测中性福尔马林固定石蜡包埋(FFPE)的非小细胞肺癌(NSCLC)组织中的PD-L蛋白,辅助鉴别可使用Keytruda治疗的NSCLC患者。研究表明,肿瘤组织样本中PD-L1表达水平越高,患者越有可能从PD-1/PD-L1抑制剂治疗中获益。肿瘤组织PD-L1表达水平评估是目前临床研究、验证和认可度最广泛的PD-1/PD-L1抑制剂疗效预测标志物,而免疫组化方法学是现阶段临床诊断级别评估肿瘤组织PD-L1表达水平的唯一方法学。
六、一位院士,三位国之名医
2019年11月22日,中国工程院开展了第14次院士增选和第13次外籍院士增选,共选举产生75位院士和29位外籍院士。其中,中国医科大学副校长、第一临床学院(附属第一医院)院长尚红教授当选中国工程院院士,成为我国第一位来自检验医学界的院士。
尚红教授主要从事艾滋病毒关键检验领域和临床检验标准领域的研究工作,在艾滋病毒储存库检测技术、预测艾滋病进展的全新标志物、我国艾滋病毒新型重组株鉴定和传播规律以及中国成人临床检验标准等方面取得系列研究成果。
2019年8月9日,由人民日报社指导,人民网、健康时报主办的国内权威的医生荣誉颁奖盛典——国家名医盛典,联合中华医学会各分会、中国医师协会各分会、中华预防医学会、国内顶级三甲医院共同发布国之名医系列榜单。首都医科大学附属北京世纪坛医院检验中心主任张曼、复旦大学附属华山医院中心实验室主任关明、四川大学华西医院实验医学科主任应斌武等三位检验医学界专家上榜。
七、从业人员的强心剂——NIPT被纳入医保
2019年6月10日,天津市医保局、卫健委公示了核定胎儿染色体非整倍体无创基因检测项目的价格,天津市医保局同时将该基因检测项目纳入了医保,明确医保支付标准。这也是首个省级(直辖市)医保局将该项目纳入医保行列。
此前,国内各省份就NIPT纳入医保均未有明确的相关规定。尽管在2015年,湖南省和贵州省均出台了关于支持基因测序技术应用的相关政策,并对部分产前检测进行了免费开放的规定,但对于孕妇无创产前检测纳入医保却未作出明确的规定。
NIPT技术被业内人士评价为“产前诊断领域的一项革命性技术”。国内的检查费用一般在一到两千元,随着技术和政策的不断完善,NIPT的降价及纳入医保关于将不断推进。但是,国家医保局也表示:受限于经济发展水平和筹资能力,基本医疗保险基金只能支付临床必需、安全有效、费用适宜的诊断、检查、治疗等费用。一些特需、非治疗性、疗效不确切、临床科研性、预防保健和价格昂贵的临床诊断、检查、治疗项目暂时还难以纳入。
八、前罗氏名将黄柏兴担任迪安诊断CEO
2019年5月,黄柏兴加入迪安诊断,成为迪安诊断董事、高级管理顾问。10月22日,正式担任迪安诊断CEO。此前,他任职罗氏中国区总经理十三年,开创了罗氏诊断中国市场增长率超140倍增长的局面,且年平均增长率稳步维持在25%以上。黄柏兴的时代,让中国成为了罗氏诊断全球第二大市场,仅次于美国。同时,他也是中国AGP(加速增长计划)的主要推动者。
九、资本寒冬下,高通量测序逆势生长
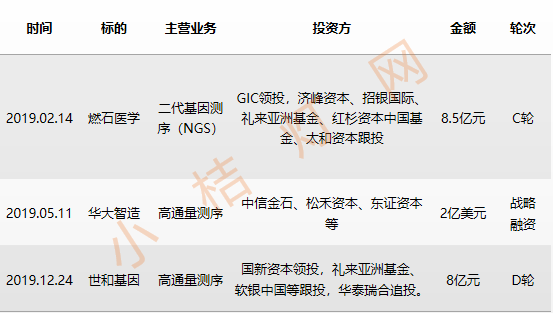
据统计,2019年体外诊断行业发生的融资事件数量不足2018年的50%,其中3笔超过8亿元的融资均发生在高通量测序领域,表现亮眼。
基因产业满足医改、民生、新经济等各项国家战略需求,被国际上许多国家认定为战略性新兴产业。基因检测作为基因产业的基础,也备受资本青睐。随着致病基因的不断发现,特别是针对癌症、感染性疾病和心血管疾病等遗传病,传统的基因检测方法已经不能满足临床需求,而高通量测序技术以其高效、便捷的特点显示出在这个领域的技术优势,因而其能够在资本寒冬中逆势生长似乎也不足为奇。
十、DRG付费来临,大批医耗供应商受影响
2019年5月24日,国家医保局发布消息,对其在5月20日召开的疾病诊断相关分组(DRG)付费国家试点工作启动视频会议上对DRG付费工作的情况进行了发布,并公布了DRG付费国家30个试点城市名单。10月16日,国家医保局印发了《疾病诊断相关分组(DRG)付费国家试点技术规范和分组方案的通知》,同时公布了《国家医疗保障DRG分组与付费技术规范和《国家医疗保障DRG(CHS-DRG)分组方案》两个技术标准,意味着我国DRG顶层设计基本完成。
疾病诊断相关组(Diagnosis Related Groups,DRG)是用于衡量医疗服务质量效率以及进行医保支付的一个重要工具。DRG 实质上是一种病例组合分类方案,即根据年龄、疾病诊断、合并症、并发症、治疗方式、病症严重程度及转归和资源消耗等因素,将患者分入若干诊断组进行管理的体系。
当DRG的支付标准成为医院盈亏的临界点时,在保证医疗质量的前提下,医院在提供医疗服务的过程中,药品和耗材的总体消耗费用离临界点越远,则医院盈余越多。可见,正在经受药品耗材零差价、两票制、全国比价挂网采购等政策挑战之中的药品和耗材供应商,将不得不面临DRG付费所带来的又一轮强势调整。
扫二维码用手机看
版权所有:湖南比扬医疗科技有限公司 企业营业执照号:91430104691832278C 地址:长沙市岳麓区学士街道黎家村路比扬科技园 湘ICP备09028240号-1 网址建设:中企动力 长沙 比扬.网址




